Summary
AMAÇProstat kanserli 16 olgu için retrospektif olarak CyberKnife (CK) ve intensity-modulated radiotherapy (IMRT) planlarını dozimetrik ve fiziksel olarak karşılaştırmaktır.
GEREÇ VE YÖNTEM
On altı hasta için IMRT ve CK karşılaştırılmasında konformite
(CI), heterojenite (HI), rektum ve mesane hacimlerinin
aldığı %100 (V100), %66 (V66), %50 (V50), %33 (V33) ve
%10'luk (V10) yüzde dozlara bakıldı.
BULGULAR
V10, V33 ve V50 rektum hacimlerinin dozları CK'da daha
düşük bulundu. Bu hacimler için p<0.001, <0.001 ve 0.019
bulundu. Rektum V66 ve V100 hacimlerinin yüzde dozları
CK'da daha yüksekti. Mesane V10 ve V33 hacimlerinin aldığı
medyan yüzde dozlar CK'da daha düşük bulundu. Mesanenin
V50 ve V60 hacimlerinin aldığı yüzde doz değerleri
IMRT'de 5.4% ve 3.45%, CK' da 13.4% ve 8.05% bulundu.
Medyan CI, IMRT'de 0,94, CK' da 1.23; HI, IMRT ve CK için
1.08 ve 1.33, p<0.001 idi.
SONUÇ
Yüksek doz bölgesinde CK tedavisi IMRT'den daha üstün bulunmuştur.
Hedef hacimde doz heterojenitesi CK planlarında
sistemin özelliğinden dolayı daha düşüktür. CI IMRT'de daha
iyiyken, kritik organ koruması CK'da daha iyidir.
Introduction
Intensity Modulated Radiation Therapy (IMRT) radyoterapide teknolojinin getirdiği son yeniliklerden biridir. IMRT tekniğinde 3 Boyutlu Konformal Radyoterapi’de (3DCRT) kullanılan Doz-Hacim Grafikleri (DVH) ve hedef-kritik organ tanımları gibi tüm terimler kullanılır. Bu nedenle IMRT tedavisi 3DCRT’nin bir uzantısı olarak düşünülebilir. Özelikle konkav şekilli hedef hacimlerde IMRT doz yoğunlukları ayarlanmış alanlar kullanıldığından daha iyi doz kapsaması elde edilir. Çoğu araştırmacı IMRT’nin baş-boyun, prostat ve servikal bölgeler için 3DCRT’den daha üstün olduğunu göstermiştir.[1-6]Prostat, IMRT için oldukça uygun bir tedavi bölgesidir. Hedef hacim içinde doz arttışı yapılırken rektum ve mesane dozları düşürülebildiğinden prostat için IMRT etkin bir tedavi tekniğidir. 3DCRT ile karşılaştırıldığında IMRT’de prostat içinde doz artışı yapılırken geç ve erken dönem toksisitenin anlamlı olarak azaldığı gösterilmiştir. [7-9] Zelefsky ve ark.[10] IMRT ile tedavi ettikleri 772 prostat hastasında IMRT ile tümör kontrol oranının arttığını, normal doku komplikasyonunun azaldığını yayınlamışlardır.
IMRT daha iyi tümör kontrol olasılığı sağlamasına rağmen tekniğin karmaşıklığından dolayı hem planlamada hem de ışınlamada daha ayrıntılı kalite kontrol programı gerektirir.[11] Hasta set-up’ındaki hatalar, sistematik hatalar ve tedavi sırasında organ hareketinden kaynaklı hatalar IMRT tedavisinin başarısını azaltır. Tedavi sırasında organ hareketi hedef hacmin yerinin değişmesine sebep olabilir. Bu durumda hedef hacim düşük doz bölgesine geçerken kritik organlar ise yüksek doz bölgesine geçebilir. Yayınlanan çoğu araştırmada prostat içine yerleştirilen fiducial işaretleyicilerin portal görüntülemesi ile belirlenen prostatanın hareketi ve klinik belirsizlikler nedeni ile PTV hacmine yeterli emniyet marjının verilmesi gerektiği gösterilmiştir.[12-14] Teknolojinin gelişim ile Image Guided RadioTherapy (IGRT), 4 Boyutlu Konformal Radyoterapi (4DCRT) ya da CyberKnife (CK) robotik radyoterapi ile IMRT tedavisi daha doğru ve etkin bir tedavi modeli olur (Şekil 1).
Sekil 1: CK robotik radyocerrahi sistemi.
Aubin ve ark.[15] prostat içine yerleştirilen altın işaretçilerin, Elektronik Portal Görüntüleme SisteAubin ve ark.[15] prostat içine yerleştirilen altın işaretçilerin, Elektronik Portal Görüntüleme Sistemi (EPID) günlük alınan rütin portal görüntülerde takipleri sonucu prostat hareketinin belirlenebileceğini yayınlamışlardır. Tedavi sırasında her gün alınacak ultrason tabanlı görüntüleme ile prostat lokalizasyonu daha iyi belirlenmesine rağmen, pratikte doktor gözetimi gerektirdiğinden kullanımı zordur.
Bununla birlikte CK sisteminde prostat içine yerleştirilen altın işaretçilerin görüntüsü ortagonal X ışını görüntüleme sistemleri ile tedavi boyunca alınabilir. Bu görüntüler planlamada oluşturulan planlama için alınmış bilgisayarlı tomogrofi (BT) görüntülerinden oluşturulmuş Digital Reconstructed Radiogrph’larla (DRR) tedavi sırasında gerçek zamanlı olarak karşılaştırılır. Altın işaretçilerin yerdeğişimi hem XYZ düzleminde hem de rotasyonel olarak belirlenir ve masanın bu yönlerindeki hareketi ile gerekli düzeltmeler yapılabilir. Bu özellik ile CK sistemi prostat kanserini 1 mm’ den az hata payı ile tedavi olanağı sağlar. Ayrıca PTV hacmine verilen emniyet marjı azaltılacağından rektum ve mesanenin aldığı dozlar minimize edilmiş olur.
CK hastaya hiç bir frame (çerçeve) takılmasına gerek kalmadan oda içersindeki ortagonal X ışını sistemleri ile görüntü rehberli radyocerrahi yapılabilen bir sistemdir. 6 MV lineer hızlandırıcı bilgisayar kontrollu robotik kola monte edilerek hedef üzerine tedavi odası içinde 1200 noktadan radyasyon gönderilebilir. Böylece yüksek doz hedef hacime doğru bir şekilde verilirken, çevre kritik organlar maksimum korunmuş olur.
Prostat tümör hücrelerin düşük α/β oranlarından dolayı doz arttırmanın yanında hipofraksiyonasyon tedavi de terapatik oranı arttırmaktadır. Prostat kanserinde hipofraksiyonun katkısını araştıran çoğu çalışmada, fraksiyon başına yüksek dozlu tedavinin normal fraksiyonlu tedavi ile aynı hatta daha iyi tümör kontrol oranı sağlanırken normal dokuda geç ve erken toksisitenin aynı kaldığı raporlanmıştır.[16,17]
Kliniğimizde prostat kanserli olgulara CK ile 5 fraksiyonda 36.25 Gy doz ya da IMRT ile 35-37 fraksiyonda toplam doz 72-74 Gy olan tedavi protokolü uygulanmaktadır. CK tedavisinde her bir fraksiyonun süresi yaklaşık 1.5-2 saat kadardır.
Bu çalışmada amaç, lokalize prostat kanserli olgular için yapılan CK ve IMRT tedavi planlarının dozimetrik ve fiziksel olarak karşılaştırmasını yapmaktır. Bu karşılaştırmada hedef hacim ve kritik organlara ait DVH’ler, konformite (CI) ve heterojenite (HI) değerleri dikkate alınmıştır.
Methods
Hastalar ve GörüntülemeBu çalışmaya TNM sınıflandırmasına (AJCCTNM Classification of Malignant Tumors, 2002) göre T1-T2 evre lokalize prostat kanserli 16 hasta dahil edildi.[18] Hastaların medyan yaş ortalaması 72 idi. Çalışmaya dahil edilen 16 hastanın 13 tanesi kliniğimizde IMRT ile geriye kalan 3 tanesi ise CK ile tedavi edildi. Tüm 16 hasta için geriye dönük olarak hem IMRT planı hem de CK planı yapılarak 16 hasta için plan karşılaştırılması yapıldı.
IMRT ile tedavi edilecek hastalar mesane dolu olarak alpha cradle ile sabitlenerek sırtüstü pozisyonda görüntülemeye alındı. BT taraması tedavi masasına eş masada beşinci lomber vertebradan ischial çıkıntıdan yaklaşık 10 cm aşağıya kadar 3 mm dilim kalınlığı ile alındı. BT taramasından sonra, her hastadan pelvik manyetik rezonans (MR) görüntüleme dahilinde özellikle prostatı belirlemek için T2 ağırlıklı 3 mm kalınlıklı MR görüntülemesi yapıldı. BT ve MR görüntüleri, hedef hacimlerin ve kritik organların belirlenmesi için Mutual Information algoritması kullanarak görüntü eşlemesi yapabilen sanal simülasyon bilgisayarına aktarıldı (FocalSim, Computed Medical System, St. Louis).
Eşleştirilmiş BT ve MR görüntüleri kullanılarak prostat hacmi hedef hacim olarak, rektum, mesane ve femur başları kritik organlar olarak deneyimli radyasyon onkoloğu tarafından belirlendi. Gross Hedef (GTV) hacmi prostata hiç marj verilmeden oluşturulurken, Klinik Hedef Hacmi (CTV) GTV hacmine her yönden 1 cm marj verilirken sadece posterior yönden rektum duvarında doz artışını engellemek için 0.5 cm marj verilerek oluşturuldu. Set-up hatalarını ve radyasyon demetinin penumbrasından gelen azalımı dikkate almak içinde Planlanlama Hedef Hacmi (PTV) ise CTV’ye 0.5 cm marj verilerek oluşturuldu. IMRT planlaması için, çizilen planlama BT görüntüleri ters (inverse) yaklaşımla IMRT planı yapabilen XiO (CMS, Compured Medical System, St. Louis) planlama bilgisayarına aktarıldı. Şekil 2’de IMRT ve CK planları için çizilen hedef hacimler ve kritik organlar gösterilmektedir.
CK ile tedavi edilecek olan prostat kanserli olgular için ayrı bir görüntüleme prosedürü olmasına rağmen,[19] çizilen hedeflerin ve kritik organların hacimlerinin IMRT planı ile aynı olması için IMRT görüntüleme protokolü ile alınan BT ve MR görüntüleri CK konturlama sistemine (Cyris Inview, Accuray, Sunnyvale, CA) gönderildi. Ters yaklaşım ile plan yapılan sistemde hedef hacimler ve kritik organlar aynı radyasyon onkoloğu tarafından BT-MR eşleştirilmiş görüntüleri ile belirlendi. CK tedavi cihazı gerçek zamanlı görüntüleme ile her tedavi bölgesi için görüntü rehberli tedavi imkanı sağlar. Kafatası takibi ile beyin tümörlü hastalara görüntü rehberli tedavi yapılırken, tedavi bölgesine yakın yerleştirilen fiducial işaretleyicilerin takibi ile de omurga ve prostat hastalarının tedavisi görüntü rehberliğinde 1 mm altında hata ile yapılır. Çalışmaya dahil edilen ve CK ile tedavi edilen 4 olguya tedaviden en az bir hafta once radyologlar tarafından prostat içine altın işaretleyiciler yerleştirildi. Planlama BT görüntüleri sırtüstü pozisyonda alpha cradle yatak içinde alındı. Genelikle, üretra foley katater kullanılarak yerleştirilen balona kontrast madde verilerek belirlendi. GTV hacimleri prostatı içine alacak şekilde marjsız olarak belirlenirken, PTV hacimleri ise GTV’ye her yönden 0.5 cm marj verilerek oluşturuldu. Kritik organların belirlenmesi IMRT planlarındaki ile aynı yapıldı.
IMRT ve CK Planları
On altı olgu için IMRT planları XiO planlama
sisteminde step and shoot tekniği kullanan 6 MV
enerjili demetlerle 41 çift yapraklı çoklu kolimatör
(MLC) sistemine sahip Siemens AvatGarde cihazı
için yapıldı. Bir olgu hariç tüm IMRT planlarında
gentri açıları 0°, 72°, 144°, 216° ve 288°
olan 5 alan kullanıldı. Sadece bir olguda hasta anatomisinden
dolayı, demet yerleşimi posterior yönden
(gentri 180°) başlanarak yapıldı. Şekil 3’de örnek
IMRT planı gösterilmektedir. Demetlerin merkezi
PTV merkezine yerleştirilip, her bir demet penumbra
etkisini bağlı doz düşüşünü azaltmak için
PTV’yi kapsayacak şekilde MLC ile şekillendirildi.
Planlar ters yaklaşımda convolution algoritması
kullanılarak, hedef hacimlere ve kritik organlara
tanımlanan doz değerleri ile bu organlara ait hesaplanan
doz değeri arasındaki farkı hesaplayan objektif
fonksiyonu minimuma (<0.001) indirilerek
tekrarlı hesaplama ile yapıldı.
Sekil 3: XiO planlama sisteminde IMRT için demet yerleşimi.
Pollack ve ark.[20] ve Zelefsky ve ark.[21] fazla sayılı hastalarla yaptıkları çalışmalarda, PSA (Prostat Spesifik Antijen) değeri >10 ng/mL olan hastalarda>74 Gy IMRT uygulandığında rektal reaksiyonlar azalırken lokal başarının anlamlı olarak arttığını bildirmişlerdir. Kliniğimizde IMRT uygulanacak prostat hastaları PTV hacmine fraksiyon dozu 2 Gy toplam doz 74 Gy olacak şekilde 37 fraksiyonda tedavi edilmektedir. Planlama sırasında hedef hacime ve kritik organlara tanımlanan doz şeması Tablo 1’de gösterilmektedir.
Tablo 1: IMRT planı için doz tanımlamaları
Yapılan planların kabulü için hedef hacimlerin ve kritik organların DVH eğrileri değerlendirilip kabul kriterlerinin sağlanması koşulu aranmıştır. Tablo 2’de kabul edilmiş bir IMRT planına ait bilgiler sunulmaktadır. XiO planlama sisteminde optimizasyon sonunda elde edilen ideal yoğunluk haritası için seçilen yoğunluk düzeyi değerine göre alan içi alancıklar (segment) oluşturulmaktadır. Tedavi süresinin ve alancıkların sayısı artmaması için yoğunluk düzeyi değeri kısıtlanmıştır. Bu değerin sınırlandırılması ile alancık sayısı 70’in altında olan ve ışınlama süresi 18 dakika olan planlar elde edilmiştir. Bilindiği gibi, step and shoot tedavi tekniğinde tedavi süresi beam on durumunu ve segmentler arası MLC hareketlerini içermektedir.[22,23]
Tablo 2: Kabul edilmiş bir IMRT planındaki hedef hacim ve kritik organ dozları
Plan değerlendirilmesi sırasında DVH değerlendirilmesinin yanında her bir BT kesitindeki doz dağılımı incelenirken CTV hacmi içinde soğuk alanın ya da normal doku bölgesinde sıcak alanın olup olmadığı da kontrol edilmiştir. Bazı olgularda plan kabul kriterleri hasta anatomisinden ya da demet enerjisinden dolayı sağlanamadığı için planın kabulu radyasyon onkoloğunun değerlendirilmesi ile olmuştur. Sonuç olarak, plan değerlendirilmesi ve kabulü aşağıdaki ölçütlere göre yapılmıştır:
1) PTV hacminin %95’i 74 Gy’i almalı ve 74
Gy’in %105’ini alan PTV hacmi <5% olmalı.
2) 70 Gy’den fazla doz alan rektum ve mesane
hacmi %10’u geçmemeli.
3) Femur başlarında maksimum doz 50 Gy’i geçmemeli.
4) Plan içindeki sıcak alan PTV hacmi ile üst üste
gelen rektum ya da mesane hacminde olmamalı.
On altı olgu için yapılan IMRT planlarında bu kriterler sağlanmaya çalışılsa da 8 planda 70 Gy’den fazla doz alan rektum ve mesane hacimleri %10’luk hacimden büyük çıkmıştır.
CK planları lineer optimizasyon algoritması kullanarak planlama yapan On-Target (Accuray, Sunnyvale) planlama sisteminde yapılmıştır. Tablo 3’de CK planları için tanımlanan doz değerleri gösterilmiştir. Planlar için medyan kolimatör boyutu 20 mm idi. CK planlarında ters yaklaşımlı tekrarlı yöntem kullanılmıştır. Kliniğimizde CK prostat kanserli olgular 5 fraksiyonda hedef hacme 36.25 Gy yani fraksiyon dozu 7.25 Gy olan tedavi protokolü ile tedavi edilmektedir. Kritik organ olan rektum ve mesane için maksimum doz 32 Gy olarak tanımlandı. Keskin doz düşüşünden dolayı femur başlarına herhangi bir doz değeri girilmemiştir. Plan değerlendirilmesi sırasında maksimum doza, %70 izodoz eğrisinin kapsadığı PTV hacmine, demetçik sayısına ve tedavi süresine bakılmıştır. Şekil 4’ de bir olguya ait CK planı gösterilmektedir.
Tablo 3: CK planları için doz tanımlaması
IMRT planları yaklaşık 5 saat içinde hazırlanmıştır. Bu süre görüntülerin transferini, eşleştirilip değerlendirilmesini, ilgili organların ve hedef hacimlerin çizilmesini, demetlerin yerleştirilmesini, doz tanımlamalarını ve olası en iyi dağılım için planlama sisteminin optimizasyonunu içermektedir. Bu süreye ek olarak hastaya özel kalite kontrol ölçümleri de eklenmelidir. Kullanılan birçok yöntem ve prosedür olmakla beraber,[11] kliniğimizde IMRT ile tedavi edilecek prostat kanserli olgularda tedavi sırasında set-up doğruluğu, iki gün ara ile alınan elektronik portal görüntülerin eşzamanlı düzeltilmesi ile yapılmaktadır.[24] IMRT planları için hastaya özel kalite kontrol ölçümlerinde mutlak doz doğrulaması 0.125 cc iyon odası ve IMRT fantomu (PTW Freiburg, Germany) ile yapılırken rölatif doz doğrulaması ise 729 tane iyon odası içeren 2D-Array (PTW Freiburg, Germany) sistemi ile yapılmaktadır.
CK tedavisi için görüntülerin çizilmesi, doz tanımlanması ve optimum planın hesaplanması yaklaşık 3-4 saat içersinde olmuştur. Sistemin özelliğinden dolayı her hastaya özel plan doğrulanması için yapılan kalite kontrol ölçümlerine gerek yoktur. CK sisteminde aylık ve haftalık olarak lineer hızlandırıcıya ve robota ait kalite kontrol ölçümlerinin yanında rando fantomlar için hazırlanan tedavi planlarının doğrulanması GafchromicTM film ile yapılmaktadır. CK sisteminde tedavi boyunca prostat içine yerleştirilen en az üç işaretleyicinin görüntülü takibi sonunda bulunan rotasyonel ya da düzlemsel sapmalar masanın bu yönlerde hareketi ile düzeltilebilmektedir. İşaretleyici takibindeki belirsizlikler görüntülerden, robotun noktalamasından ve tedavi planlamasında hedef hacmin lokalizasyonundaki belirsizliklerle birleşebilir.
Tedavi Planlarının Karşılaştırılması
IMRT planlarında PTV hacmine maksimum doz
olarak 74 Gy’in %5’i minimum olarak da 74 Gy’in %1’i tanımlanıp, PTV hacminin %95’inin 74 Gy’i
alması hedeflenmiştir. Bunun yanında 70 Gy’i geçen
rektum ve mesane hacimlerinin %10’dan az
olmasına çalışılmıştır.
Şekil 6’da kabul edilmiş bit IMRT planı gösterilmektedir. 16 olgu için yapılan IMRT ve CK planlarının karşılaştırılmasında CI ve HI,[25,26] %100, %66, %50, %33 ve %10 rektum ve mesane hacimlerinin aldığı yüzde dozlara bakılmıştır. Bu hacimler V100, V66, V50, V33 ve V10 olarak isimlendirilmiştir. Femur başının aldığı doz CK planlarında anlamsız olduğunda karşılaştırmaya dahil edilmemiştir.
Konformite ve homojenite indeksleri aşağıdaki gibi tanımlanmıştır:
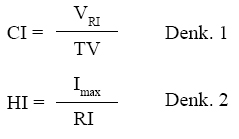
Burada VRI tanımlanan dozun kapsadığı PTV hacmini, TV toplam PTV hacmini, Imax PTV hacmindeki maksimum dozu ve RI ise PTV hacmine tanımlanan dozu işaret etmektedir. Farklılıklar Student’s t-testi ile istatiksel olarak değerlendirilmiştir. P<0.05 değeri anlamlı farklılığı ifade etmektedir.
Results
Klinik olarak kabul şartları sağlanırken yeterli PTV kapsaması sağlanacak şekilde yapılan 16 olguya ait IMRT ve CK planları değerlendirildi. Çalışmanın amacından dolayı yapılan planların karşılaştırılmasında dozimetrik ve fiziksel değerlere bakıldı. Şekil 4 ve Şekil 5’te aynı hastaya ait yapılan IMRT ve CK planları gösterilmektedir. CK planlarında PTV hacmini %95’ini kapsamak için planlar medyan olarak %75 izodoz hattına normalize edildi. İki planın doz dağılımı karşılaştırıldığında CK planlarında hızlı doz değişimi IMRT planlarına göre fazladır. Aynı hastaya ait DVH karşılaştırması Şekil 6’da görülebilir.Sekil 4: CK tedavi planlama sistemi.
Sekil 5: Bir hastaya ait IMRT planı ve DVH eğrisi.
Sekil 6: Bir hasta için CK ve IMRT planları DVH eğrilerinin karşılaştırılması.
Her iki planın istatiksel olarak karşılaştırılması Tablo 4’de sunulmaktadır. PTV hacmine ait medyan konformite indeksi IMRT ve CK planları için sırasıyla 0.94 ve 1.23 (p<0.001) olarak bulunmuştur. Her iki sistemde PTV hacmi kapsanmasında oldukça başarılıdır. Yapılan planların PTV hacmi içindeki homojenite indeksine bakıldığında IMRT planlarındaki homojenite CK planlarından daha fazla 1’e yakındır. Medyan homojenite indeksi IMRT ve CK planlarında sırasıyla 1.08 ve 1.33 (p<0.001) olarak bulunmuştur. PTV hacmi içinde heterojen doz dağılımı oluşması CK sisteminin doğal özelliğidir. Bu özelliği ile PTV hacmi içinde tümör yoğunluğu (aktivitesi) fazla noktalarda doz arttırmaya olanak sağlar.
Normal dokuların karşılaştırmasında %10, %33, %50, %66 ve %100 rektum ve mesane hacimlerinin aldığı yüzde doz değerlerine bakıldı. V10, V33, and V50 rektum hacimlerinin aldığı doz değerleri CK planlarında daha düşük bulundu. Bu hacimlere ait p değerleri sırasıyla <0.001, <0.001 ve 0.019 bulundu. Fakat V66 ve V100 rektum hacimlerinin aldığı doz değerleri CK planlarında daha yüksek çıktı. Bu hacimlere ait IMRT planlarındaki doz değerleri sırasıyla %12.73 ve %2.015 iken CK planlarında %20.95 ve %2.6 olarak bulundu. CK planlarında V10 ve V33 mesane hacimlerinin aldığı doz değerleri CK planlarında oldukça düşük çıktı. Bu doz değerleri IMRT planında %96.25 ve %33.75 iken CK planlarında %47.8 ve %23.75 hesaplandı (p<0.001 ve p=0.047). IMRT planlarında mesanenin V50 ve V66 hacimlerinin aldığı doz CK planlarından daha düşük bulundu. Bu yüzde doz değerleri IMRT planlarında %5.4 ve %3.45 iken CK planlarında %13.4 ve %8.05 olarak bulundu. Şekil 7’de tüm hastalara ait rektum ve mesane dozlarının karşılaştırılması sunulmaktadır.
Sekil 7: Tüm hastalara ait her iki plandaki kritik organ dozları.
Discussion
Yapılan bu çalışmada kliniğimizde tedavi gören prostat olgulu hastaların IMRT ve CK planlarının fiziksel ve dozimetrik olarak karşılaştırılması yapılmıştır. Çalışmada plan karşılaştırılması hedef kapsanması, konformite ve homojenite indeksi, mesane ve rektum dozlarının dikkate alınması ile yapılmıştır.Sonuçlarımız göstermiştir ki; IMRT planlarında konformite ve homojenite CK planlarından daha iyidir. IMRT’de hedef hacim daha iyi kapsanabilirken, yüksek doza maruz kalan mesane ve rektum hacimleri CK planında elde edilenlerden daha fazladır. CK sistemi mesane ve rektum koruması özellikle yüksek doz bölgesinde daha başarılıdır. Bu durum Şekil 6’da gösterilmektedir. CK sisteminin robotik kolundan dolayı oda içersinde 1200 noktadan hasta ışınlanabilir. Bu nedenle CK sisteminde mesane ve rektumda düşük doz alan hacimler IMRT’den daha yüksek çıkmıştır. Bu durum mesane ve rektumun toplam dozu hesaplanırken dikkate alınmalıdır.
Çalışmamızda CK planlarında IMRT ile karşılaştırıldığında daha heterojen doz dağılımı oluştuğu gösterilmiştir. Klasik yaklaşımla radyoterapide PTV hacminin homojen doz dağılımı ile kapsanması önemlidir. Bununla birlikte, prostat içinde tümörün hipoksik olduğu bölgelerde prostatın tamamına verilen dozdan daha fazla doz verilmek istenebilir. CK sisteminde PTV içinde homojen olmayan doz dağılımı elde edilebildiğinden hipoksik bölgelerde doz artışı oluşturularak tedavi başarısı arttırılabilir.
Yapılan çalışmalarda prostat hareketleri ve gerekli emniyet marjları detaylıca incelenmiştir. Bu çalışmalarda gösterildiği gibi, prostatın anteriorposterior yönündeki hareketi diğer yönlere göre daha baskındır.[14,27-28] IMRT planlarında PTV hacmi, prostat hacmine posterior yönden 0.5 cm diğer yönlerden 1 cm marj verilerek oluşturulmuştur. Böylece set-up hataları göz önüne alınmıştır. Çalışmaya dahil edilen tüm olgularda dolu mesane ile görüntüleme yapılıp, tedavi sırasında da mesane doldurulmuştur. Böylece prostat hareketinin minimuma indirilmesi ve plan sırasında mesane korumasının arttırılması amaçlanmıştır. Tüm IMRT hastalarının tedavi süresinde pozisyon doğrulaması iki gün ara aile alınan portal görüntülemeler ile DRR görüntülerinin eşleştirilmesi sonucu belirlenen kemik yapıların kaymasına bakılarak yapılmıştır. Bununla birlikte IMRT planları için PTV hacmine verilen marjdan dolayı mesane ve rektum organlarının aldığı dozlar artmaktadır. CK planlarında PTV prostat hacmine 0.5 cm marj verilerek oluşturulmuştur. Ayrıca, prostat hareketini tedavi sırasında gerçek zamanlı takip etmek için prostat içine 4 tane işaretleyici yerleştirilmiştir. Tedavi sırasında belli aralıklarla alınan ortogonal X ışını görüntüleri ile işaretleyicilerin dolayısıyla prostatın sapması belirlenir ve masa hareketi ile gerçek zamanlı düzeltme yapılmıştır. Bu nedenle PTV’ye verilen marj azaldığından rektum ve mesane dozları da düşürülmüş olur.
IMRT ile konformite artmasına rağmen, tedavi sırasındaki set-up ve hedef hacmin hareketinden kaynaklı hatalardan dolayı ve uzun tedavi gününden dolayı uygulamada CK sistemine göre sınırlamalar oluşmaktadır. Prostat tedavisinin doğruluğu IGRT, 4DCRT ve CK tekniklerinin kullanılması ile arttırılabilir. Bu çalışmada prostat kanserinin radyobiyolojisi ile ilgili araştırılma yapılmamasına rağmen, yapılan çoğu çalışmada prostat tümörünün düşük α/β değerine sahip olmasından dolayı hipofraksiyone uygun olduğu gösterilmiştir.[28,29] Bu nedenle CK tedavisinde prostat kanserli olgularda hipofraksiyone tedavi uygulandığından tümör kontrol oranı arttırılabilir.
Sonuç olarak, çalışmamızda CK sisteminin sahip olduğu özelliklerden dolayı prostat tedavisi CK ile doğru bir şekilde yapılabileceği, etkin tedavi modellerine alternatif olarak kullanılabileceği gösterilmiştir.
References
1) Ashman JB, Zelefsky MJ, Hunt MS, Leibel SA, Fuks
Z. Whole pelvic radiotherapy for prostate cancer using
3D conformal and intensity-modulated radiotherapy.
Int J Radiat Oncol Biol Phys 2005;63(3):765-71.
2) Luxton G, Hancock SL, Boyer AL. Dosimetry and radiobiologic
model comparison of IMRT and 3D conformal
radiotherapy in treatment of carcinoma of the
prostate. Int J Radiat Oncol Biol Phys 2004;59:267-84.
3) Vlachaki MT, Teslow TN, Amosson C, Uy NW, Ahmad
S. IMRT versus conventional 3DCRT on prostate
and normal tissue dosimetry using an endorectal
balloon for prostate immobilization. Med Dosim
2005;30(2):69-75.
4) James HV, Scrase CD, Poynter AJ. Practical experience
with intensity-modulated radiotherapy. Br J Radiol
2004;77;3-14.
5) Bucci MK, Bevan A, Roach M 3rd. Advances in radiation
therapy: conventional to 3D, to IMRT, to 4D, and
beyond. CA Cancer J Clin 2005;55(2):117-34.
6) van de Bunt L, Van der Heide UA, Ketelaars M, de
Kort GAP, Jürgenliemk-Schulz IM. Conventional,
conformal, and intensity-modulated radiation therapy
treatment planning of external beam radiotherapy for
cervical cancer: The impact of tumor regression. Int J
Radiation Oncology Biol Phys 2006;64(1);189-96.
7) De Meerleer G, Vakaet L, Meersschout S, Villeirs G,
Verbaeys A, Oosterlinck W, et al. Intensity-modulated
radiotherapy as primary treatment for prostate cancer:
acute toxicity in 114 patients. Int J Radiat Oncol Biol
Phys 2004;60(3):777-87.
8) Gert De Meerleer, Luc Vakaet, Werner R. T. De Gersem
et al. Radiotherapy of prostate cancer with or without
intensity modulated beams: a planning comparison. Int.
J. Radiation Oncology Biol Phys 2000;47(3);639-648.
9) Sethi A, Mohideen N, Leybovich L, Mulhall J. Role
of IMRT in reducing penile doses in dose escalation
for prostate cancer. Int J Radiat Oncol Biol Phys
2003;55(4):970-8.
10) Zelefsky MJ, Fuks Z, Happersett L, Lee HJ, Ling CC,
Burman CM, et al. Clinical experience with intensity
modulated radiation therapy (IMRT) in prostate cancer.
Radiother Oncol 2000;55(3):241-9.
11) Ezzell GA, Galvin JM, Low D, Palta JR, Rosen I, Sharpe
MB, et al. Guidance document on delivery, treatment
planning, and clinical implementation of IMRT: report of the IMRT Subcommittee of the AAPM Radiation
Therapy Committee. Med Phys 2003;30(8):2089-115.
12) Boehmer D, Maingon P, Poortmans P, Baron MH, Miralbell
R, Remouchamps V, et al. Guidelines for primary
radiotherapy of patients with prostate cancer. Radiother
Oncol 2006;79(3):259-69.
13) Andrew O. Jones and Marc T. Kleiman. Patient setup
and verification for intensity-modulated radiation therapy
(IMRT). Med Dosim 2003;28(3):175-83.
14) Nederveen AJ, van der Heide UA, Dehnad H, van
Moorselaar RJ, Hofman P, Lagendijk JJ. Measurements
and clinical consequences of prostate motion
during a radiotherapy fraction. Int J Radiat Oncol Biol
Phys 2002;53(1):206-14.
15) Aubin M, Liu Y, Langen KM, et al. Set-up verification
using portal images of implanted markers: An inter-observer
study. Abstract 44th Annual ASTRO Meeting.
16) Brenner DJ. Hypofractionation for prostate cancer radiotherapy-
what are the issues? Int J Radiat Oncol Biol
Phys 2003;57(4):912-4.
17) Fowler JF, Ritter MA, Chappell RJ, Brenner DJ. What
hypofractionated protocols should be tested for prostate
cancer? Int J Radiat Oncol Biol Phys 2003;56(4):1093-104.
18) Galvin JM, Ezzell G, Eisbrauch A, Yu C, Butler B,
Xiao Y, et al. Implementing IMRT in clinical practice:
a joint document of the American Society for Therapeutic
Radiology and Oncology and the American Association
of Physicists in Medicine. Int J Radiat Oncol
Biol Phys 2004;58(5):1616-34.
19) Carlo Cavedon, Joseph Stancanello, Paolo Francescon
et al. Spelized imaging techniques for cyberknife treatment
planning. Chapter 9 of Robotic Radiosurgery
Volume 1. 2005: 81-94.
20) Pollack A, Zagars GK, Starkschall G, Antolak JA,
Lee JJ, Huang E, et al. Prostate cancer radiation
dose response: results of the M. D. Anderson phase
III randomized trial. Int J Radiat Oncol Biol Phys
2002;53(5):1097-105.
21) Zelefsky MJ, Fuks Z, Hunt M, Yamada Y, Marion C,
Ling CC, et al. High-dose intensity modulated radiation
therapy for prostate cancer: early toxicity and biochemical
outcome in 772 patients. Int J Radiat Oncol
Biol Phys 2002;53(5):1111-6.
22) Adams EJ, Convery DJ, Cosgrove VP, McNair HA,
Staffurth JN, Vaarkamp J, et al. Clinical implementation
of dynamic and step-and-shoot IMRT to treat
prostate cancer with high risk of pelvic lymph node
involvement. Radiother Oncol 2004;70(1):1-10.
23) Livi L, Paiar F, Banci-Buonamici F, Simontacchi G,
Detti B, Gacci M, et al. Localized prostate cancer
treated with intensity-modulated radiotherapy. Tumori 2006;92(3):197-201.
24) Melian E, Mageras GS, Fuks Z, Leibel SA, Niehaus
A, Lorant H, et al. Variation in prostate position quantitation
and implications for three-dimensional conformal
treatment planning. Int J Radiat Oncol Biol Phys
1997;38(1):73-81.
25) Wu VW, Kwong DL, Sham JS. Target dose conformity
in 3-dimensional conformal radiotherapy and
intensity modulated radiotherapy. Radiother Oncol
2004;71(2):201-6.
26) Feuvret L, Noël G, Mazeron JJ, Bey P. Conformity
index: a review. Int J Radiat Oncol Biol Phys
2006;64(2):333-42.
27) Teh BS, Bastasch MD, Wheeler TM, Mai WY, Frolov
A, Uhl BM, et al. IMRT for prostate cancer: defining
target volume based on correlated pathologic volume of
disease. Int J Radiat Oncol Biol Phys 2003;56(1):184-91.





